ТЕРМОДИНАМИКА И СТРОЕНИЕ ПОВЕРХНОСТНОГО СЛОЯ.
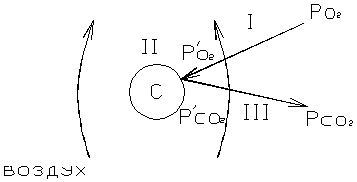
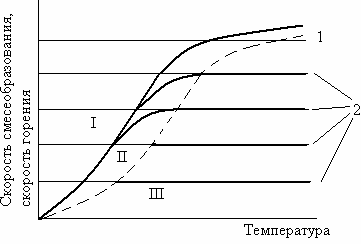
Что такое поверхностная энергия Гиббса, причины ее возникновения, ее математическое выражение и причины ее влияния на устойчивость гетерогенных дисперсных систем? Реакции в гетерогенных системах протекают на поверхности раздела фаз, причем их скорость зависит от площади этой поверхности. Поэтому все особенности гетерогенных реакций определяются поверхностными явлениями.



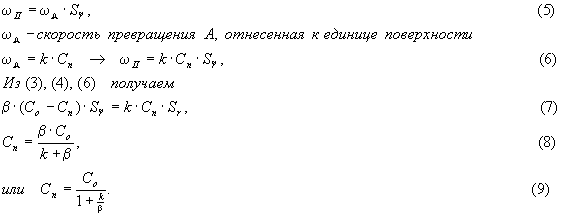







Аналогично определяются поверхностнаяэнтропия свободная П. Их численные значения зависятот положения разделяющей поверхности, к-рое для плоских поверхностей обычновыбирается из условия равенства нулю адсорбции одного из компонентов эквимолекулярнаяповерхность. В однокомпонентной системе уд. Поверхностное натяжение связаны ур-нием Гиббса - Гельмгольца:. Для границы жидкость - газ - уд.
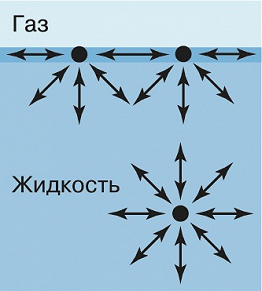







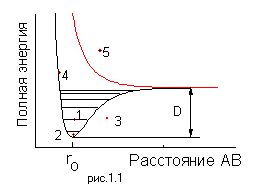
Поверхностная энергия , также свободная поверхностная энергия , поверхностная энергия Гиббса — термодинамическая функция, характеризующая энергию межмолекулярного взаимодействия частиц на поверхности раздела фаз с частицами каждой из контактирующих фаз. Другое определение поверхностной энергии — это потенциальная энергия , которая сосредоточена на межфазной поверхности границе раздела фаз , необходимая для образования единицы площади поверхности. Является избыточной по сравнению с энергией в объёме, то есть не равной нулю. Существование свободной поверхностной энергии вместе с поверхностным натяжением является причиной возникновения метастабильных состояний состояний переохлаждения, пересыщения. Свободная поверхностная энергия G s при постоянном давлении совпадает с термодинамической функцией — энергией Гиббса , характеризующей состояние поверхности раздела фаз в гетерогенных системах.